技術・研究材料紹介(企業広告)
“光る”ヒト肝セルライン(CYP3A4G/7R HepaRG®)のご紹介
株式会社ケー・エー・シー 試薬事業部 橋本静香
ヒト肝腫瘍由来のセルラインである「HepaRG®」は,従来の肝セルラインと比較して,薬物代謝酵素活性など肝特異的機能を高く保持しており,ヒト初代肝細胞に近いセルラインである.ロット差が少なく,入手・取扱いが容易なため,薬物動態・安全性試験のスクリーニングに多く使用されている.今回は,HepaRG®に光る遺伝子を導入した新しい「光るHepaRG®」(CYP3A4G/7R HepaRG®)について紹介する.
HepaRG®は,2002年,INSERM(フランス国立衛生医学研究所)の研究チームにより,C型肝炎ドナーの肝腫瘍部位から樹立された細胞株である.DMSOを含む培地で約2週間培養すると分化し,このときのHepaRG®細胞の形態は,肝細胞様細胞と胆管上皮細胞が1:1の割合となる,非常にユニークな形態を示す(Fig.1).分化したHepaRG®は,CYPs,PhaseⅡ酵素,トランスポーター,核内レセプターを高レベルに発現し,胎児肝および腫瘍マーカーのα-Fetoproteinを発現せず,アルブミンを発現するなど,成人肝細胞の特徴を示す.薬物動態試験および安全性試験は,分化後のHepaRG®を用いて実施される.
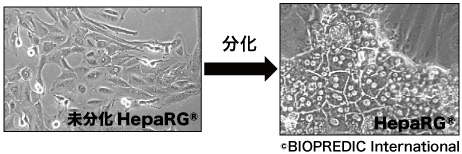
Fig.1 HepaRG®の細胞形態
HepaRG®の薬物動態研究分野での使用例としては,酵素誘導試験の実績が最も多く,CYP1A2,CYP2B6,CYP3A4の主要なCYPsやUGT1A1等の抱合酵素,トランスポーター誘導の報告もあり,誘導性評価のスクリーニングにおける有用性は多くの論文で示されている.また,代謝試験や毒性試験での研究報告も多い.特に,毒性試験の使用実績は,酵素誘導試験に次いで多く,Acetaminophen等を用いた細胞毒性評価や小核試験などの遺伝毒性試験での研究成果が続々と報告されている.その他,3次元培養を実施した研究報告も増えつつあり,2002年の細胞株樹立以降,HepaRG®は薬物動態・安全性研究分野で多くの研究に用いられ,その有用性が報告されている.現在市販されているHepaRG®は「分化済みHepaRG®凍結バイアル」,または「未分化細胞と分化用培地のセット(ユーザーの手元で増殖・分化させて使用)」の製品で,いずれも分化後のHepaRG®を試験に供することとなっている.しかしながら,これまでHepaRG®の分化成熟度の判別については,細胞の形態変化を指標にするしかなかった.
より客観的な分化成熟度の判別に向けて,2014年,辻らは,HepaRG®にCYP3A4およびCYP3A7の制御領域下に蛍光レポーター遺伝子を接続したBACベクターを導入し,成熟肝細胞で発現するCYP3A4を緑色蛍光で,胎児肝細胞で発現するCYP3A7の発現を赤色蛍光で検出できる,新しい「光るHepaRG®」を開発した(以下,CYP3A4G/7R HepaRG®と示す).CYP3A4G/7R HepaRG®は,CYP3A7を発現する未分化状態では赤色の蛍光を発し,DMSOを含む分化用培地で培養して分化させると,CYP3A4を発現し緑色蛍光を発した(Fig.2).この結果より,HepaRG®の分化成熟度を緑と赤の色調変化で客観的に判断することが可能となり,最適な分化状態を蛍光量で判断し試験を遂行することができる.また,CYP3A4G/7R HepaRG®は,肝分化因子の探索や高効率肝分化条件の検討など,再生医療分野研究への使用も期待される.さらに,筆者らは,CYP3A4の発現が緑色蛍光で検出できる本細胞の特徴を生かし,CYP3A4G/7R HepaRG®を用いたCYP3A4誘導性試験を行い,CYP3A4の各種誘導剤の添加により,CYP3A4G/7R HepaRG®の緑色蛍光が増加することを確認した(なお,ラット・マウスのCyp3aの誘導剤であるPCNについて誘導は認められなかった)(Fig.3).この結果は,CYP3A4G/7R HepaRG®の緑色蛍光強度の変化を計測することにより,簡単にCYP3A4誘導を評価できる可能性を示している.さらに,筆者らは,FACSを用いて,CYP3A4G/7R HepaRG®の緑色蛍光発現細胞を単離することにも成功した(Fig.4).この結果は,通常,胆管上皮細胞と肝細胞様細胞が混在しているHepaRG®細胞の中から,CYP3A4活性の高い細胞(肝細胞)を単離して試験に供する可能性を示しており,HepaRG®を用いた薬物代謝試験,安全性試験への応用が期待される.
HepaRG®の注目度は高く,本細胞を用いた研究報告は毎年続々と発表されている.新しい「光るHepaRG®」であるCYP3A4G/7R HepaRG®は,従来製品とともに創薬研究,再生医療研究を発展させる有用なツールになると期待される.
参考文献:Tsuji S et al.,:Dual-Color Fluorescence Imaging to Monitor CYP3A4 and CYP3A7 Expression in Human Hepatic Carcinoma HepG2 and HepaRG Cells. PLOS ONE. 2014 Aug 7; 9(8):e104123.
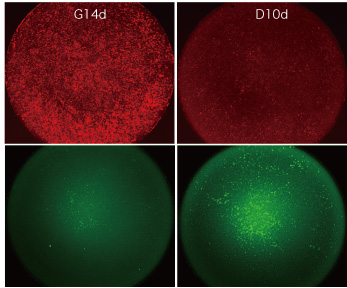
Fig.2 CYP3A4G/7R HepaRG®
左:未分化HepaRG® 右:HepaRG®(分化済み)
分化に伴い赤色蛍光が減少し(上段)緑色蛍光(下段)が増加
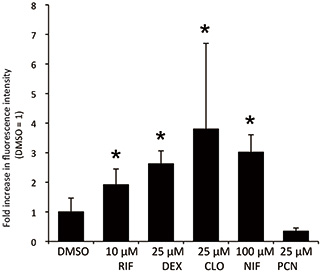
Fig.3 CYP誘導剤で誘導時のCYP3A4G/7R HepaRG ®(分化後)の緑色蛍光量の変化
各誘導剤添加により、蛍光量の有意な増加(*:p<0.05)が見られた。
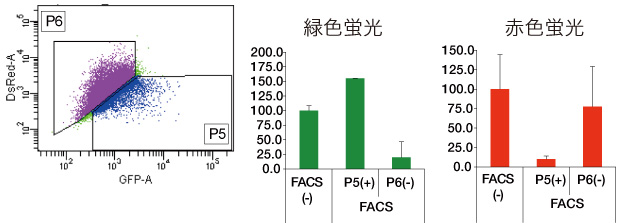
Fig.4 FACSにより、緑色蛍光細胞
(CYP3A4陽性細胞)を単離
